Informações do produto
|
Nome do produto |
Gato.Não |
Especificações. |
|
Kit de ensaio de proliferação celular Click-iT EdU-594 |
G1603 |
100 T |
Introdução
É um método de avaliação comum e importante nas ciências da vida para julgar a influência de certos genes, medicamentos, etc. em células cultivadas in vitro, analisando a capacidade de proliferação celular, ou para analisar o crescimento e a capacidade de renovação de células de tecidos individuais sob diferentes estados. ou intervenções de estimulação. . Atualmente, existem muitos métodos para detectar a proliferação celular. A maioria deles usa algumas enzimas metabólicas produzidas pelas células para avaliar indiretamente a atividade de proliferação das células (como o método CCK-8, o método MTT, etc.), mas alguns medicamentos ou o estado das próprias células terão um certo impacto sobre os resultados da avaliação. A detecção direta da síntese de DNA em células para determinar a proliferação celular é reconhecida como o método de detecção mais preciso e eficaz. No entanto, tanto o método de incorporação de nucleósidos radiomarcados inicialmente utilizado como o subsequente método BrdU melhorado baseado na detecção de anticorpos têm certas limitações.
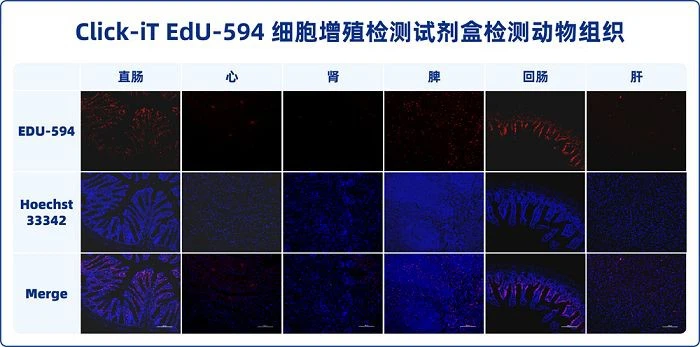
EdU (5-etinil-2'-desoxiuridina) é um análogo da timidina contendo um grupo acetileno que, quando injetado em animais ou incubado com células in vitro, essas pequenas moléculas podem se difundir rapidamente em vários órgãos e tecidos, penetrar nas células e pode ser incorporado ao DNA recém-sintetizado no lugar da timidina (T) durante a proliferação celular. O grupo acetileno na molécula EdU pode sofrer uma reação de "clique" com a sonda de azida marcada com fluorescência sob a catálise de íons de cobre para formar um anel triazol estável, de modo que o DNA recém-sintetizado possa ser marcado com a sonda fluorescente correspondente. Comparado com o método de incorporação de nucleosídeos radiomarcados, o método de detecção EdU não tem limitações como contaminação radioativa; em comparação com o método de detecção de BrdU, o método de detecção de EdU não requer tratamento de desnaturação de DNA, nem requer reação antígeno-anticorpo, o que reduz bastante a complexidade do experimento e do tempo, e o torna mais eficiente em termos de tempo, mais responsivo, mais estável e mais preciso. Este kit pode ser usado para detectar a proliferação celular em células cultivadas in vitro ou em tecidos animais. A sonda fluorescente neste kit é de fluorescência vermelha com comprimento de onda máximo de excitação de 593 nm e comprimento de onda máximo de emissão de 614 nm. Após a marcação das células em proliferação, o núcleo apresentará fluorescência vermelha brilhante e os núcleos serão marcados com um corante nuclear convencional (o corante nuclear Hoechst 33342 é fornecido neste kit). A intensidade de fluorescência da população de células cultivadas in vitro também pode ser detectada por citometria de fluxo, e a atividade de replicação do DNA na fase S do ciclo celular pode ser avaliada de acordo com a intensidade de fluorescência.
Condições de armazenamento e manuseio
Transporte com gelo molhado; armazene a -20 graus no escuro. O reagente catalítico EdU (reagente A) e o tampão de reação podem ser armazenados a 4 graus; o período de validade é de 12 meses.
Componentes
|
Número do componente |
Componente |
G1603-100T |
|
G1603-1 |
Solução de armazenamento EdU (10 mM) |
100 μL |
|
G1603-2 |
Catalisador (Reagente A) |
120 μL |
|
G1603-3 |
Coloração fluorescente iF594 (Reagente B) |
50 μL |
|
G1603-4 |
Aditivo Catalítico (Reagente C) |
2×100 mg (pó) |
|
G1603-5 |
Tampão de reação |
20ml |
|
G1603-6 |
Corante Hoechst 33342 |
30 μL |
|
Manual de instruções |
1 unidade |
|
Observação: os tempos de reação acima correspondem à 96-detecção de placa de poço.
Preparação do experimento
1. Meio de cultura celular contendo soro;
2. Solução de permeabilização: buffer contendo 0.2-0,5% Triton X-100 (recomendado G1204);
3. Fixador: paraformaldeído 4% (recomendado G1101) ou outros reagentes similares;
4. Buffer PBS (recomendado G4202);
5. Água ultrapura;
6. Modelagem animal e reagentes relacionados à seção de tecido (detecção de proliferação de células de tecido animal).
Passos
1. Amostras de células in vitro e preparação de reagentes:
1.1. As células são plantadas uniformemente na placa de cultura celular a uma certa densidade (a densidade de plantio é determinada por fatores como tamanho da célula, velocidade de crescimento, etc.) e depois que as células aderem à parede ou retornam ao estado normal, execute estimulação de drogas correspondente e outros tratamentos (como detecção de suspensão. Células, siga a operação de rotina das células em suspensão, e todo o experimento precisa adicionar etapas como centrifugação).
1.2. O aditivo catalítico (reagente C) foi centrifugado em baixa velocidade, dissolvido em 1 mL de água ultrapura e armazenado a -20 grau para uso posterior.
2. Rotulagem EdU, fixação e permeabilização de células in vitro:
2.1. Prepare a solução de trabalho de incubação 2× EdU: adicione 2 μL de solução estoque de EdU (10 mM) a cada 1 mL de meio de cultura celular completo, que é 20 μM de solução de trabalho de incubação 2× EdU, e coloque-a em uma incubadora para pré-aquecer (é recomendado explorar com concentração de trabalho EdU de 10 μM em experimentos preliminares);
2.2. No modo de troca de meio meio, metade do meio de cultura celular original na placa de cultura foi removido por sucção, e um volume igual de solução de trabalho de incubação 2×EdU pré-aquecida foi adicionado por um determinado período de tempo (o tempo de incubação geralmente depende do crescimento celular correspondente). O ciclo celular geralmente é responsável por cerca de 10% do ciclo celular. Para a maioria das células aderentes e de crescimento rápido, recomenda-se incubar durante cerca de 2 horas. A situação específica precisa ser ajustada de acordo com as características das células e a situação real após o tratamento. Se for necessário incubar por mais tempo A concentração de trabalho do EdU pode ser reduzida adequadamente por um curto período de tempo; a concentração de EdU pode ser aumentada adequadamente durante um período de tempo mais curto);
2.3. Lave as amostras de células marcadas com EdU e incubadas com tampão PBS por 1-2 vezes, adicione fixador para cobrir as células e fixe-as em temperatura ambiente por 15 minutos (se a detecção de fluxo for necessária, anexe as células antes desta etapa. Digerir e ressuspender e depois fixar e depois seguir o método de tratamento de células suspensas); lave 2-3 vezes com buffer PBS, 3-5 min de cada vez;
2.4. Remover o tampão PBS, adicionar solução de permeabilização para cobrir células ou tecidos e incubar à temperatura ambiente durante 15 min;
2.5. Depois de remover o permeabilizador, lave 1-2 vezes com tampão PBS por 3-5 min de cada vez e depois vá para a etapa 4.
3. Modelagem de injeção Animal EdU e processamento de seção de tecido:
3.1. De acordo com os requisitos experimentais, uma ou mais injeções de EdU foram realizadas em animais por injeção intraperitoneal, injeção intramuscular, injeção subcutânea e injeção na veia da cauda. O valor depende do conteúdo da pesquisa e das condições do animal. Este kit fornece algumas soluções de armazenamento de EdU, que são usadas principalmente para rotulagem de células EdU in vitro. Se a modelagem EdU for necessária para animais, os reagentes EdU (recomendado G5059) podem ser encomendados separadamente;
3.2. As células do tecido epitelial, como o intestino delgado, proliferam rapidamente e as células do tecido, como o cérebro, proliferam lentamente. As partes de tecido de crescimento rápido são geralmente marcadas por menos de 12 horas, enquanto o tecido de crescimento lento pode levar vários dias para ser marcado; o melhor tempo de marcação é baseado em Depende do experimento específico. Devido à rápida proliferação do tecido epitelial do intestino delgado, recomenda-se tomar este tipo de tecido como referência de marcador;
3.3. Após os animais modelo terem sido sacrificados de acordo com os padrões prescritos, os tecidos necessários foram retirados e secções congeladas ou secções de parafina foram feitas de acordo com procedimentos de rotina;
um. Para cortes congelados: retornar à temperatura ambiente, adicionar uma quantidade adequada de fixador e fixar à temperatura ambiente por 15 minutos. Remova o fixador e lave 3 vezes com uma quantidade adequada de tampão PBS por 3-5 min de cada vez; remova o tampão PBS, use uma quantidade apropriada de solução de permeabilização e incube à temperatura ambiente por 10-15 min; remova a solução de permeabilização e lave com tampão PBS por 1- 2 vezes, 3-5 min de cada vez, depois vá para a etapa 4.
b. Para seções de parafina: Desparafinize as seções, reidrate e lave com PBS por 5 min. Remover o tampão PBS, adicionar solução de permeabilização, cobrir as células ou tecidos e incubar à temperatura ambiente durante 15 minutos; após remover a solução de permeabilização, lave com tampão PBS 1-2 vezes por 3-5 minutos de cada vez e depois vá para a etapa 4.
4. Resposta de clique do EdU:
4.1. Durante a fixação e perfuração de células ou tecidos, prepare a solução de reação de clique (consulte o protocolo na tabela abaixo para diferentes sistemas de preparação de amostras)
Para células cultivadas in vitro: esta etapa de referência corresponde ao volume de 10 96-amostras de placas de poços (100 μL por poço). O volume do preparo pode ser aumentado ou diminuído em proporções iguais de acordo com a necessidade de uso. Adicione os componentes na ordem mostrada na tabela. Adicione borda e misture bem (atualmente preparada e usada);
|
Componente |
Volume |
|
Tampão de reação |
935 μL |
|
Catalisador (Reagente A) |
10 μL |
|
Coloração fluorescente iF594 (Reagente B) |
5 μL |
|
Aditivo Catalítico (Reagente C) |
50 μL |
|
Volume total |
1000 μL |
Para fatias de tecido e células: Consulte o sistema abaixo para a preparação da solução de reação clique. O volume de preparação pode ser aumentado ou diminuído em proporções iguais de acordo com o número de amostras cortadas. Cada amostra de fatia é coberta com cerca de 100-200 μL de solução de reação de clique.
|
Componente |
Volume |
|
Tampão de reação |
928 μL |
|
Catalisador (Reagente A) |
10 μL |
|
Coloração fluorescente iF594 (Reagente B) |
12 μL |
|
Aditivo Catalítico (Reagente C) |
50 μL |
|
Volume total |
1000 μL |
4.2. Remova o tampão PBS na etapa anterior (etapa 2,5 ou 3,3), adicione a solução de reação clique, agite suavemente para garantir que a solução de reação cubra completamente as células ou tecidos e incubar à temperatura ambiente por 30 min no escuro;
4.3. Remova a solução de reação de clique e lave com tampão PBS 2-3 vezes por 3-5 min de cada vez (se não houver outros requisitos especiais, a intensidade de fluorescência pode ser detectada pelo citômetro de fluxo ou o efeito de fluorescência pode ser detectado por outros instrumentos).
5. Coloração de núcleos:
5.1. Remova o tampão PBS da etapa anterior, dilua a solução de coloração Hoechst 33342 e o tampão PBS na proporção de 1:500-1000, adicione as células de cobertura e incubar por 5 min;
5.2. Remova a solução de coloração Hoechst 33342 e lave com tampão PBS 2-3 vezes, 3-5 min de cada vez.
6. Análise de imagem e detecção
Coloque diretamente as células cultivadas in vitro ou amostras de fatias de tecido em um microscópio de fluorescência ou microscópio confocal e outros instrumentos para detecção para analisar a proporção de células em proliferação; ou coletar células cultivadas in vitro e usar um citômetro de fluxo para detectar a intensidade de fluorescência (recomenda-se usar uma amostra de células marcadas com EdU foi usada como controle negativo para detecção de citometria de fluxo, e uma voltagem apropriada foi selecionada), e o A atividade de replicação do DNA na fase S do ciclo celular foi avaliada de acordo com a intensidade de fluorescência. As propriedades espectrais correspondentes ao corante fluorescente iF594 (reagente B) neste kit são Ex/Em: 593 nm/614 nm (vermelho); as propriedades espectrais correspondentes à solução de coloração Hoechst 33342 são Ex/Em: 346 nm/460 nm (azul)
Observação
1. Para células cultivadas in vitro, a concentração específica de EdU e o tempo de incubação podem ser ajustados adequadamente dependendo da amostra e do objetivo da pesquisa.
2. Algumas células do tecido proliferam lentamente. A fim de excluir fatores como efeito de modelagem deficiente, recomenda-se selecionar amostras de tecido com proliferação rápida como amostras de referência (como tecido intestinal).
3. Se a cor de fundo for muito escura, isso pode ser causado por lavagem insuficiente no experimento, longo tempo de fixação de amostras de tecido e fixador residual.
4. O reagente de adição catalítica EdU (reagente C) é fácil de ser oxidado, evite exposição prolongada ao ar. Depois de preparado em solução aquosa, recomenda-se armazenar em embalagens separadas; após o teste, se a cor do reagente de adição catalítica EdU mudar ligeiramente, o sistema catalítico da reação click permanecerá o mesmo. Pode ser realizado normalmente, se ficar marrom indica que o componente falhou, descarte-o.
5. Use jaleco e luvas descartáveis durante a operação.
Somente para uso em pesquisa!
Tag: kit de ensaio de proliferação celular click-it edu-594, China fabricantes, fornecedores, fábrica de kits de ensaio de proliferação celular click-it edu-594