Introdução do produto
|
Nome do produto |
Gato.Não. |
Especificações. |
|
Kit de extração de DNA genômico de planta MagBind |
G3621-50T |
50T |
Descrição/Introdução
Usando esferas magnéticas superparamagnéticas especialmente desenvolvidas para extração e purificação de ácidos nucleicos e sistema tampão de lise especialmente otimizado, este kit pode extrair com segurança, rapidez e eficiência DNA genômico de alta pureza de 50-100 mg de amostras de tecido vegetal (como trigo, folhas de milho, etc). O tecido vegetal pode liberar rapidamente o DNA genômico após a lise e remover efetivamente as impurezas, exceto o ácido nucleico da amostra. Este kit não requer fenol, clorofórmio e outros reagentes orgânicos e não requer centrifugação em várias etapas. O DNA genômico extraído pode ser usado em reações de PCR subsequentes, reações de digestão enzimática, hibridização Southern, RAPD, AFLP, RFLP e muitos experimentos convencionais de biologia molecular.
Condições de armazenamento e manuseio
A RNase A é enviada com gelo úmido e armazenada a -20 grau; Os demais reagentes são enviados e armazenados em temperatura ambiente; A data de validade é de 12 meses.
Conteúdo do produto
|
Número do componente |
Componente |
G3621-50T |
|
G3621-1 |
Tampão PGL1 |
30ml |
|
G3621-2 |
Tampão PGL2 |
5ml |
|
G3621-3 |
Buffer GB |
30ml |
|
G3621-4 |
Tampão GD |
16ml |
|
G3621-5 |
PW do buffer |
24ml |
|
G3621-6 |
Contas SweMag |
2×1 mL |
|
G3621-7 |
RNase A |
1ml |
|
G3621-8 |
Tampão TE |
10ml |
|
Manual |
Uma cópia |
|
Antes de começar (leia com atenção)
1. Se o tampão PGL1 precipitar, aqueça-o a 65 graus e use-o quando for restaurado à temperatura ambiente.
2. Antes de usar, adicione 24 mL de etanol anidro ao Tampão GD e 56 mL de etanol anidro ao Tampão PW, misture bem e use.
3. Suporte magnético auto-fornecido.
Protocolo/Procedimentos de Ensaio
1. Lise de amostras de tecidos vegetais:
um. Quebra de moagem de lisado + moedor: (recomendado) Adicione 50{{10}} μL de tampão PGL1 a um tubo de moagem sem nuclease de 2,0 mL (recomendado HT-200-M) com antecedência e, em seguida, adicione esferas de aço inoxidável de 3-4 4 mm (recomendado G0104-200G). Em seguida, transfira rapidamente 50-100 mg de tecido vegetal fresco ou criopreservado para o tubo de moagem (amostras de folhas são cortadas em 0,5 cm2, raízes e caules são cortados em 0,5 cm). Coloque o tubo de moagem no moedor (recomendado KZ-5F-3D) e triture (procedimento de moagem recomendado: ajuste a frequência para 70 HZ, triture por 30 segundos de cada vez, repetindo o processo {{19 }} vezes com intervalo de 5 segundos entre cada moagem. Se a amostra for difícil de moer, como raízes e caules, você pode aumentar os tempos de moagem para 30 ou mais) até que a moagem esteja concluída. homogeneizado (se o tecido não for completamente homogeneizado, isso afetará o rendimento e a qualidade do DNA). Após a moagem completa, adicione 20 μL de RNase A ao tubo de moagem, misture de cabeça para baixo e incube a 65 graus por 15 min, misturando de cabeça para baixo a cada 5 min.
b. Nitrogênio líquido + Moedor Quebra de moagem: Transfira rapidamente 50-100 mg de tecido vegetal fresco ou criopreservado para um tubo de moagem sem nuclease de 2,0 mL (recomendado HT-200-M, as amostras de folhas são cortadas em 0,5 cm2, raízes e caules são cortados em 0,5 cm) contendo contas de zircônia de 3~4 3 mm (recomendado G0203-150G) e pré-resfriado com nitrogênio líquido. Coloque o tubo de moagem no moedor (recomendado KZ-5F-3D) (pré-resfrie rapidamente o adaptador em nitrogênio líquido antes de colocar o tubo de moagem) e triture até que esteja completamente em pó (se o tecido não estiver completamente reduzido a pó, afetará o rendimento e a qualidade do DNA). Em seguida, adicione 500 μL de tampão PGL1 e misture bem, adicione 20 μL de RNase A ao tubo de moagem, misture de cabeça para baixo e incube a 65 graus por 15 min, misturando de cabeça para baixo a cada 5 min.
c. Nitrogênio líquido + quebra de moagem de argamassa: Transfira rapidamente 50-100 mg de tecido vegetal fresco ou criopreservado para uma argamassa pré-resfriada com nitrogênio líquido (amostras de folhas são cortadas em 0,5 cm2, raízes e caules são cortados em 0,5 cm). Adicione nitrogênio líquido e triture o tecido com um pilão, adicionando nitrogênio líquido continuamente até que esteja completamente em pó (se o tecido não estiver completamente moído em pó, isso afetará o rendimento e a qualidade do DNA). Em seguida, transfira as amostras em pó para um tubo de centrífuga sem nuclease de 1,5 mL contendo 500 μL de tampão PGL1 e misture bem. E adicione 20 μL de RNase A ao tubo de centrífuga, misture de cabeça para baixo e incube a 65 graus por 15 min, misturando de cabeça para baixo a cada 5 min.
d. Nitrogênio líquido + bastão de pilão Quebra de moagem: Transfira rapidamente 50-100 mg de tecido vegetal fresco ou criopreservado para um tubo de centrífuga de 1,5 mL sem nuclease pré-resfriado com nitrogênio líquido (amostras de folhas são cortadas em 0,5 cm2 , raízes e caules são cortados em 0,5 cm). Adicione nitrogênio líquido e triture o tecido com um pilão, adicionando nitrogênio líquido continuamente até que esteja completamente em pó (se o tecido não estiver completamente moído em pó, isso afetará o rendimento e a qualidade do DNA). Em seguida, adicione 500 μL de tampão PGL1 ao tubo de centrífuga e misture bem. E adicione 20 μL de RNase A ao tubo de centrífuga, misture de cabeça para baixo e incube a 65 graus por 15 min, misturando de cabeça para baixo a cada 5 min.
2. Adicione 100 μL de tampão PGL2 ao tubo de centrífuga, misture bem e coloque no gelo por 5 min.
3. Centrifugar a 12,000 rpm por 5 min a 4 graus, transferir o sobrenadante para um novo tubo de centrífuga sem nuclease de 2,0 mL (se ainda houver matéria flutuante no sobrenadante obtido, é necessário centrifugar novamente a 12,000 rpm por 5 min a 4 graus e transferir o sobrenadante para outro novo 2,0 mL Tubo de centrífuga sem nuclease, nota: o sobrenadante obtido não deve exceder 500 μL).
4. Adicione Buffer GB da mesma quantidade de volume de líquido sobrenadante ao sobrenadante da etapa anterior, inverta-o totalmente e misture bem.
5. Adicione o mesmo volume de isopropanol à mistura da etapa anterior, totalmente de cabeça para baixo e misture bem. Em seguida, adicione 40 μL de SweMag Beads (as SweMag Beads devem ser dispersas uniformemente antes do uso) e misture bem com uma pipeta ou oscilação em vórtice.
6. Deixe em temperatura ambiente por 10 minutos e, durante o processo de colocação, use a pipeta para soprar ou vórtice para misturar várias vezes para manter as SweMag Beads em suspensão.
7. Transfira o tubo da centrífuga para o suporte magnético e deixe repousar por 30 s. Quando o sobrenadante estiver claro, aspire e descarte o sobrenadante.
8. Adicione 600 μL de Tampão GD, remova o suporte magnético, use uma pipeta para soprar ou vórtex até que as SweMag Beads estejam bem dispersas. Transfira o tubo da centrífuga para o suporte magnético e deixe repousar por 30 s. Quando o sobrenadante estiver claro, aspire e descarte o sobrenadante.
9. Adicione 700 μL de Tampão PW, remova o suporte magnético, use uma pipeta para soprar ou vórtex até que as SweMag Beads estejam bem dispersas. Transfira o tubo da centrífuga para o suporte magnético e deixe repousar por 30 s. Quando o sobrenadante estiver claro, aspire e descarte o sobrenadante.
10. Repita a etapa 9.
11. Abra a tampa do tubo de centrífuga e deixe-o em temperatura ambiente por 5-10 min, para que o etanol residual possa ser completamente evaporado (evite a secagem excessiva das SweMag Beads, o que pode afetar o rendimento do ácido nucleico).
12. Remova o suporte magnético, adicione 80-100 μL de Tampão TE ou Água Sem Nuclease ao tubo de centrífuga, use uma pipeta para soprar suavemente ou vórtex até que as SweMag Beads estejam bem dispersas. Fique em temperatura ambiente por 5 min.
13. Transfira o tubo de centrífuga para o suporte magnético até que as SweMag Beads estejam totalmente adsorvidas e absorva o sobrenadante em um novo tubo de centrífuga de 1,5 mL sem Nuclease para obter DNA de alta pureza.
Observação
1. Leia atentamente o manual do produto antes de usar.
2. Tente usar tecido vegetal fresco para garantir o rendimento e a integridade do DNA genômico.
3. As amostras de plantas criopreservadas devem evitar congelamentos e descongelamentos repetidos, caso contrário a qualidade e o rendimento do DNA extraído serão reduzidos.
4. Para tecidos vegetais com alto teor de ácidos nucleicos, a quantidade inicial de amostras de tecidos vegetais pode ser adequadamente reduzida para torná-los totalmente lisados; para amostras com baixo teor de ácido nucleico, a quantidade inicial de amostras de tecido vegetal pode ser aumentada adequadamente para obter uma concentração mais elevada de DNA genômico.
5. Evite congelar suspensões de esferas magnéticas durante o armazenamento. As esferas magnéticas são fáceis de assentar e devem ser totalmente agitadas no vórtex antes do uso para mantê-las em suspensão uniforme.
6. Antes de adicionar esferas magnéticas à amostra, os reagentes da amostra precisam ser bem misturados.
7. O etanol deve ser completamente evaporado antes da eluição do DNA para evitar a influência do etanol residual nas experiências a jusante.
8. Não seque as esferas magnéticas por muito tempo para evitar afetar a eficiência da eluição do DNA.
Agendar
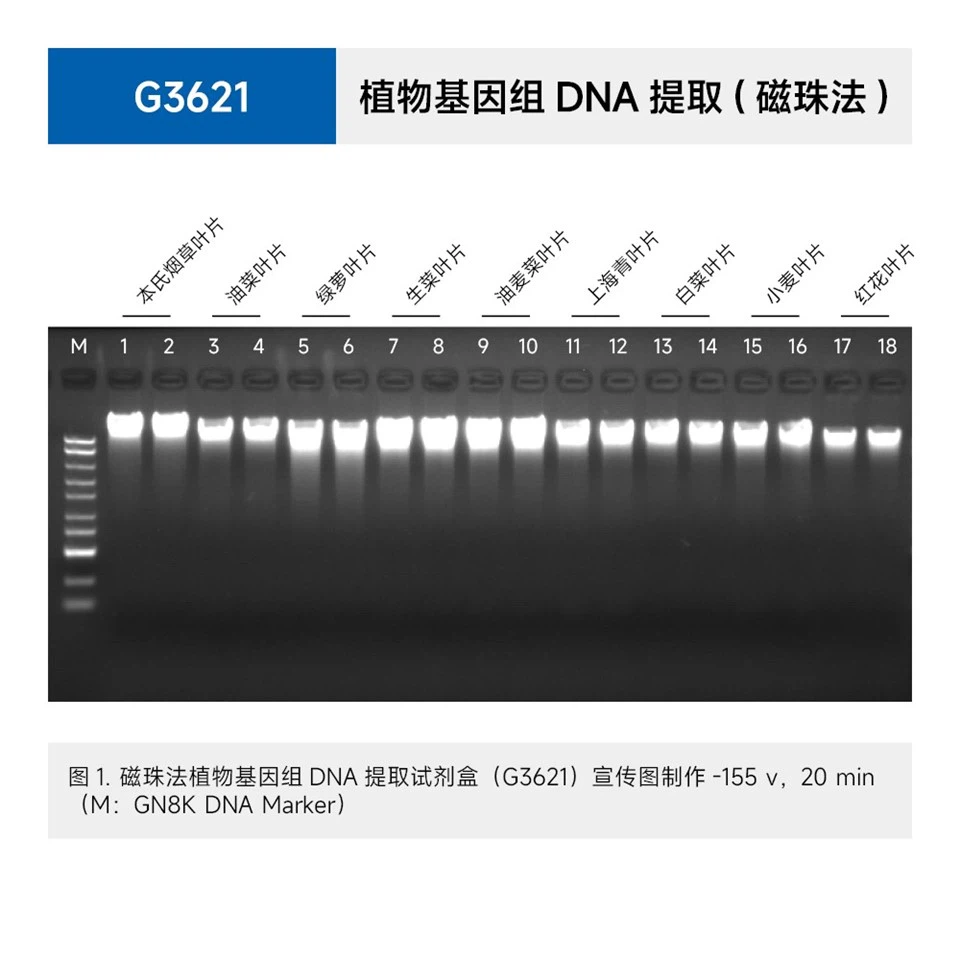
O rendimento de DNA genômico extraído de muitas amostras simples de plantas por este kit é mostrado na tabela abaixo. O rendimento do DNA genômico está relacionado às espécies de plantas, órgãos e status de crescimento. A tabela a seguir é apenas para referência.
|
Nome da amostra |
Tamanho da amostra |
Rendimento de DNA |
|
Folha de Triticum aestivum |
50mg |
25-30 ug |
|
Folha de Nicotiana benthamiana |
80mg |
7-10 ug |
|
Folha de Carthamus tinctorius |
100mg |
2-5 ug |
|
Folha de Brassica napus |
100mg |
5-10 ug |
|
Folha de Epipremnum aureum |
100mg |
5-8 ug |
|
Lactuca sativa L. var. folha de ramosa |
100mg |
55-65 ug |
|
Folha de Lactuca sativa |
100mg |
35-40 ug |
|
Folha de Brassica chinensis |
100mg |
30-35 ug |
|
Folha de Brassica pekinensis |
100mg |
20-25 ug |
Somente para uso em pesquisa!
Tag: kit de extração de DNA genômico de planta magbind, China fabricantes de kit de extração de DNA genômico de planta magbind, fornecedores, fábrica